Comprar planes
Comprar tu propia cobertura
Planes a través de tu empleador
Conoce sobre los beneficios médicos, dentales, de farmacia y voluntarios que tu empleador puede ofrecer.
Aprender
¿Buscas cobertura de Medicare?
Tratamiento del melanoma ocular uveal (PDQ®) : Tratamiento - información para profesionales de salud [NCI]
Esta información es producida y suministrada por el Instituto Nacional del Cáncer (NCI, por sus siglas en inglés). La información en este tema puede haber cambiado desde que se escribió. Para la información más actual, comuníquese con el Instituto Nacional del Cáncer a través del Internet en la página web http://cancer.gov o llame al 1-800-4-CANCER.
Información general sobre el tratamiento del melanoma ocular uveal
Incidencia y mortalidad
El melanoma de tracto uveal (iris, cuerpo ciliar y coroides), aunque es poco frecuente, es la neoplasia maligna primaria de ojo más común en los adultos. La media de incidencia ajustada por edad del melanoma uveal en los Estados Unidos es de cerca de 4,3 casos nuevos por millón de personas y no hay una variación definida relacionada con la latitud geográfica. Los hombres tienen una incidencia más alta (4,9 casos por millón) que las mujeres (3,7 casos por millón).[
Por lo general, el melanoma uveal se diagnostica a una edad avanzada; la tasa de incidencia específica por edad asciende de modo progresivo, y llega a su máximo alrededor de los 70 años.[
Los factores de susceptibilidad del huésped relacionados con la formación de este cáncer son los siguientes:[
- Raza o etnia: blanca.
- Ojos claros.
- Piel clara.
- Piel que se broncea.
Debido a estos factores de susceptibilidad, en varios estudios de observación se intentó explorar la relación entre la exposición a la luz solar y el riesgo de melanoma uveal. Hasta la fecha, solo se encontraron conexiones débiles o resultados contradictorios en estos estudios.[
Localización anatómica
Los melanomas uveales surgen en el tracto uveal anterior (iris) o en el tracto uveal posterior (cuerpo ciliar o coroides).[
La mayoría de los melanomas uveales son completamente asintomáticos al principio. A medida que el tumor se agranda, es posible que produzca distorsión de la pupila (melanoma de iris), visión borrosa (melanoma de cuerpo ciliar) o disminución marcada de la agudeza visual debido a un desprendimiento de retina secundario (melanoma de coroides). A veces se produce desprendimiento seroso de la retina. Si hay desprendimiento extenso, en ocasiones se presenta un glaucoma de ángulo cerrado secundario. Desde el punto de vista clínico, hay varias lesiones con características similares al melanoma uveal, incluso un carcinoma metastásico, la escleritis posterior y los tumores benignos, como los nevos y los hemangiomas.[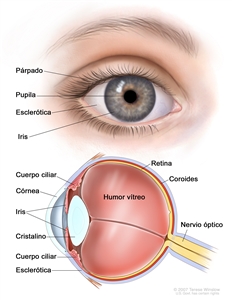
Diagnóstico
El examen minucioso por parte de un médico con experiencia continúa siendo la prueba más importante para diagnosticar un melanoma ocular. Un melanoma uveal pequeño no se puede diferenciar de un nevo. A menudo, se observa el crecimiento de lesiones uveales pequeñas antes de diagnosticar un melanoma. Los hallazgos clínicos que sirven para identificar un melanoma son los siguientes:[
- Pigmento anaranjado en la superficie tumoral.
- Líquido subretiniano.
- Tumor que mide más de 2 mm de grosor.
- Reflectividad interna baja en la ecografía.
Las pruebas complementarias para el diagnóstico, como la angiografía fluorescente y la ecografía, son muy valiosas para determinar o corroborar el diagnóstico.[
Factores pronósticos
Hay varios factores que influyen en el pronóstico. Los factores más importantes son los siguientes:
- Tipo celular. Para obtener más información, consultar la sección Clasificación celular del melanoma ocular uveal.
- Tamaño del tumor.
- Localización del margen anterior del tumor.
- Grado de compromiso del cuerpo ciliar.
- Diseminación extraocular.
Varias características microscópicas adicionales afectan el pronóstico del melanoma ocular, incluso las siguientes:
- Actividad mitótica.
- Infiltración linfocítica.
- Asas fibrovasculares (posiblemente).
Después de una enucleación, el factor pronóstico de desenlace que más se usa es el tipo celular: los melanomas de células fusiformes A conllevan el mejor pronóstico y los melanomas de células epitelioides conllevan el pronóstico más desfavorable.[
El compromiso extraocular, la recidiva y la metástasis se relacionan con un pronóstico muy precario y no se prevé la supervivencia a largo plazo.[
Referencias:
- Singh AD, Topham A: Incidence of uveal melanoma in the United States: 1973-1997. Ophthalmology 110 (5): 956-61, 2003.
- Inskip PD, Devesa SS, Fraumeni JF: Trends in the incidence of ocular melanoma in the United States, 1974-1998. Cancer Causes Control 14 (3): 251-7, 2003.
- Singh AD, Bergman L, Seregard S: Uveal melanoma: epidemiologic aspects. Ophthalmol Clin North Am 18 (1): 75-84, viii, 2005.
- Weis E, Shah CP, Lajous M, et al.: The association between host susceptibility factors and uveal melanoma: a meta-analysis. Arch Ophthalmol 124 (1): 54-60, 2006.
- Harris RB, Griffith K, Moon TE: Trends in the incidence of nonmelanoma skin cancers in southeastern Arizona, 1985-1996. J Am Acad Dermatol 45 (4): 528-36, 2001.
- Uveal melanoma. In: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. Springer; 2017, pp 805–17.
- Yap-Veloso MI, Simmons RB, Simmons RJ: Iris melanomas: diagnosis and management. Int Ophthalmol Clin 37 (4): 87-100, 1997 Fall.
- Eye and ocular adnexa. In: Rosai J: Ackerman's Surgical Pathology. 8th ed. Mosby, 1996, pp 2449-2508.
- Albert DM, Kulkarni AD: Intraocular melanoma. In: DeVita VT Jr, Lawrence TS, Rosenberg SA: Cancer: Principles and Practice of Oncology. 9th ed. Lippincott Williams & Wilkins, 2011, pp 2090-8.
- Shields CL, Furuta M, Berman EL, et al.: Choroidal nevus transformation into melanoma: analysis of 2514 consecutive cases. Arch Ophthalmol 127 (8): 981-7, 2009.
- Gragoudas ES, Egan KM, Seddon JM, et al.: Survival of patients with metastases from uveal melanoma. Ophthalmology 98 (3): 383-9; discussion 390, 1991.
- Introduction to melanocytic tumors of the uvea. In: Shields JA, Shields CL: Intraocular Tumors: A Text and Atlas. Saunders, 1992, pp 45-59.
Clasificación celular del melanoma ocular uveal
Los melanomas oculares primarios surgen de los melanocitos del tracto uveal.[
- Células fusiformes A (células fusiformes con núcleos delgados y sin nucléolos visibles).
- Células fusiformes B (células fusiformes con núcleos más grandes y nucléolos definidos).
- Células epitelioides (células poligonales más grandes, con uno o más nucléolos prominentes).
- Células intermedias (similares a las células epitelioides, pero más pequeñas).
La mayoría de los melanomas oculares primarios contienen proporciones variables de células epitelioides, fusiformes A y fusiformes B (melanomas de células mixtas). Los melanomas primarios puros de células epitelioides son infrecuentes (casi el 3 % de los casos).[
Referencias:
- Klintworth GK, Scroggs MW: The eye and ocular adnexa. In: Sternberg SS, ed.: Diagnostic Surgical Pathology. Lippincott Williams & Wilkins, 1999, pp 994-6.
- Grossniklaus HE, Green WR: Uveal tumors. In: Garner A, Klintworth GK, eds.: Pathobiology of Ocular Disease: A Dynamic Approach. 2nd ed. M. Dekker, 1994, pp 1423-77.
- Histopathologic characteristics of uveal melanomas in eyes enucleated from the Collaborative Ocular Melanoma Study. COMS report no. 6. Am J Ophthalmol 125 (6): 745-66, 1998.
Clasificación e información sobre los estadios para el melanoma ocular uveal
Tamaño tumoral
El melanoma uveal a menudo tiene una configuración nodular o en forma de cúpula pero, en ocasiones, hay tumores planos o difusos con poca elevación que comprometen amplias áreas de la úvea.
Las clasificaciones del tamaño tumoral de acuerdo con los límites utilizados en un Collaborative Ocular Melanoma Study (COMS), son las siguientes:[
- Pequeño: la altura apical oscila entre 1,0 mm y 3,0 mm y el diámetro basal mayor mide de 5,0 mm a 16,0 mm.[
1 ] - Mediano: la altura apical oscila entre 3,1 mm y 8,0 mm y el diámetro basal mayor mide hasta 16,0 mm.[
2 ] - Grande: la altura apical mide más de 8,0 mm, o el diámetro basal mide más de 16,0 mm cuando la altura apical mide por lo menos 2,0 mm.
Aunque la mayoría de los melanomas oculares tienen una configuración elevada, cerca del 5 % crecen con una distribución difusa que quizás también tenga importancia pronóstica. Los tumores tienen una configuración de crecimiento plano horizontal, con un espesor de cerca del 20 % o menos que la dimensión basal máxima. Esta variante poco común del melanoma uveal parece tener un pronóstico más precario; en particular, cuando el diámetro es grande y los márgenes están mal definidos.[
En la práctica clínica, la base del tumor se calcula según el promedio de diámetros de disco óptico (1 dd = 1,5 mm). El promedio de elevación se puede calcular en dioptrías (3 dioptrías = 1 mm). Se deben emplear otras técnicas, como la ecografía, para obtener mediciones más precisas.
Una función importante de la ecografía oftálmica es la detección de la diseminación extraescleral.[
Enfermedad metastásica
Las metástasis sistémicas son evidentes solo en el 2 % al 3 % de los pacientes en el momento del diagnóstico de un melanoma ocular primario.[
Las metástasis sistémicas por lo general tienen origen hematógeno y el primer sitio donde se suelen encontrar es el hígado.[
Es muy infrecuente que los melanomas de coroides de cualquier tamaño invadan el nervio óptico o las meninges.[
Estadificación
Agrupamiento por estadios y definiciones TNM del American Joint Committee on Cancer
El American Joint Committee on Cancer (AJCC) designó los estadios mediante la clasificación TNM (tumor, ganglio linfático y metástasis) para definir el melanoma de tracto uveal.[
Al igual que en la 7.a edición del AJCC Cancer Staging Manual, no hay un sistema de estadificación para los melanomas de iris en la 8.a edición. No obstante, se debe registrar la clasificación TNM para este sitio y esta combinación histológica.
| Categoría T | Criterios T |
|---|---|
| a Reproducción autorizada de AJCC: Uveal melanoma. En: Amin, MB, Edge Sb, Greene FL et al., eds.:AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 805–17. | |
| b Los melanomas de iris se originan en esta región de la úvea y predominan en esta. Si menos de la mitad del volumen tumoral está dentro del iris, es posible que el origen del tumor sea el cuerpo ciliar y se debe considerar clasificarlo como tal. | |
| TX | Tumor primario no evaluable. |
| T0 | Sin indicios de tumor primario. |
| T1 | Tumor limitado al iris. |
| –T1a | Tumor limitado al iris y tamaño no mayor de 3 horas. |
| –T1b | Tumor limitado al iris y tamaño mayor de 3 horas. |
| –T1c | Tumor limitado al iris con glaucoma secundario. |
| T2 | Tumor que confluye o se disemina en el cuerpo ciliar, la coroides o ambos. |
| –T2a | Tumor que confluye o se disemina en el cuerpo ciliar, sin glaucoma secundario. |
| –T2b | Tumor que confluye o se disemina en el cuerpo ciliar y la coroides, sin glaucoma secundario. |
| –T2c | Tumor que confluye o se disemina en el cuerpo ciliar, la coroides o ambos, con glaucoma secundario. |
| T3 | Tumor que confluye o se disemina en el cuerpo ciliar, la coroides o ambos, con diseminación escleral. |
| T4 | Tumor con diseminación extraescleral. |
| –T4a | Tumor con diseminación extraescleral y el diámetro mayor mide ≤5 mm. |
| –T4b | Tumor con diseminación extraescleral y el diámetro mayor mide >5 mm. |
| Categoría N | Criterios N |
|---|---|
| a Reproducción autorizada de AJCC: Uveal melanoma. En: Amin, MB, Edge Sb, Greene FL et al., eds.:AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 805–17. | |
| NX | Ganglios linfáticos regionales no evaluables. |
| N0 | Sin compromiso de ganglios linfáticos regionales. |
| N1 | Metástasis en ganglios linfáticos regionales o depósitos tumorales separados en la órbita. |
| –N1a | Metástasis en uno o más ganglios linfáticos regionales. |
| –N1b | Sin compromiso de ganglios linfáticos regionales, pero con depósitos tumorales separados en la órbita que no son contiguos al ojo (coroides y cuerpo ciliar). |
| Categoría M | Criterios M |
|---|---|
| a Reproducción autorizada de AJCC: Uveal melanoma. En: Amin, MB, Edge Sb, Greene FL et al., eds.:AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 805–17. | |
| M0 | Sin metástasis a distancia según la clasificación clínica. |
| M1 | Metástasis a distancia. |
| –M1a | El diámetro mayor de la metástasis más grande mide ≤3,0 cm. |
| –M1b | El diámetro mayor de la metástasis más grande mide 3,1–8,0 cm. |
| –M1c | El diámetro mayor de la metástasis más grande mide ≥8,1 cm. |
| Categoría | Tamaño tumoral |
|---|---|
| a Adaptación de AJCC: Uveal melanoma. En: Amin, MB, Edge Sb, Greene FL et al., eds.:AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 805–17. | |
| 1 | El tumor mide ≤12 mm de diámetro y ≤3 mm de grosor;o |
| El tumor mide ≤9 mm de diámetro y 3,1–6 mm de grosor. | |
| 2 | El tumor mide 12,1–18 mm de diámetro y ≤3 mm de grosor;o |
| El tumor mide 9,1–15 mm de diámetro y 3,1–6 mm de grosor;o | |
| El tumor mide ≤12 mm de diámetro y 6,1–9 mm de grosor. | |
| 3 | El tumor mide 15,1–18 mm de diámetro y 3,1–6 mm de grosor;o |
| El tumor mide 12,1–18 mm de diámetro y 6,1–9 mm de grosor;o | |
| El tumor mide ≤18 mm de diámetro y 9,1–12 mm de grosor;o | |
| El tumor mide ≤15 mm de diámetro y 12,1–15 mm de grosor. | |
| 4 | El tumor mide >18 mm de diámetro y tiene cualquier grosor;o |
| El tumor mide 15,1–18 mm de diámetro y >12 mm de grosor;o | |
| El tumor mide ≤15 mm de diámetro y >15 mm de grosor. | |
| Estadio | TNM | Descripción |
|---|---|---|
| T = tumor primario; N = ganglio linfático regional; M = metástasis a distancia. | ||
| a Reproducción autorizada de AJCC: Uveal melanoma. En: Amin, MB, Edge Sb, Greene FL et al., eds.:AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 805–17. | ||
| b 1) Los melanomas primarios de cuerpo ciliar y coroides se clasifican a partir de cuatro categorías de tamaño tumoral según el grosor y el diámetro. Consultar el Cuadro 4. 2) En la práctica clínica, se calcula el diámetro basal mayor del tumor en diámetros de disco óptico (DD; en promedio, 1 DD = 1,5 mm), y el grosor del tumor se calcula en dioptrías (en promedio, 2,5 dioptrías = 1 mm). La ecografía y la fotografía del fondo de ojo se usan para obtener mediciones más exactas. 3) Cuando se registran las mediciones histopatológicas después de la fijación, a veces se subestiman el diámetro y el grosor del tumor debido a la reducción del tejido. | ||
| I | T1a, N0, M0 | –T1a = tamaño tumoral de categoría 1 sin compromiso del cuerpo ciliar ni diseminación extraocular. |
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| Estadio | TNM | Descripción |
|---|---|---|
| T = tumor primario; N = ganglio linfático regional; M = metástasis a distancia. | ||
| a Reproducción autorizada de AJCC: Uveal melanoma. En: Amin, MB, Edge Sb, Greene FL et al., eds.:AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 805–17. | ||
| b 1) Los melanomas primarios de cuerpo ciliar y coroides se clasifican a partir de cuatro categorías de tamaño tumoral según el grosor y el diámetro. Consultar el Cuadro 4. 2) En la práctica clínica, se calcula el diámetro basal mayor del tumor en diámetros de disco óptico (DD; en promedio, 1 DD = 1,5 mm), y el grosor del tumor se calcula en dioptrías (en promedio, 2,5 dioptrías = 1 mm). La ecografía y la fotografía del fondo de ojo se usan para obtener mediciones más exactas. 3) Cuando se registran las mediciones histopatológicas después de la fijación, a veces se subestiman el diámetro y el grosor del tumor debido a la reducción del tejido. | ||
| IIA | T1b–d, N0, M0 | –T1b = tamaño tumoral de categoría 1 con compromiso del cuerpo ciliar. |
| –T1c = tamaño tumoral de categoría 1 sin compromiso del cuerpo ciliar, pero con diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| –T1d = tamaño tumoral de categoría 1, con compromiso del cuerpo ciliar y diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| T2a, N0, M0 | –T2a = tamaño tumoral de categoría 2 sin compromiso del cuerpo ciliar ni diseminación extraocular. | |
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| IIB | T2b, N0, M0 | –T2b = tamaño tumoral de categoría 2 con compromiso del cuerpo ciliar. |
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| T3a, N0, M0 | –T3a = tamaño tumoral de categoría 3 sin compromiso del cuerpo ciliar ni diseminación extraocular. | |
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| Estadio | TNM | Descripción |
|---|---|---|
| T = tumor primario; N = ganglio linfático regional; M = metástasis a distancia. | ||
| a Reproducción autorizada de AJCC: Uveal melanoma. En: Amin, MB, Edge Sb, Greene FL et al., eds.:AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 805–17. | ||
| b 1) Los melanomas primarios de cuerpo ciliar y coroides se clasifican a partir de cuatro categorías de tamaño tumoral según el grosor y el diámetro. Consultar el Cuadro 4. 2) En la práctica clínica, se calcula el diámetro basal mayor del tumor en diámetros de disco óptico (DD; en promedio, 1 DD = 1,5 mm), y el grosor del tumor se calcula en dioptrías (en promedio, 2,5 dioptrías = 1 mm). La ecografía y la fotografía del fondo de ojo se usan para obtener mediciones más exactas. 3) Cuando se registran las mediciones histopatológicas después de la fijación, a veces se subestiman el diámetro y el grosor del tumor debido a la reducción del tejido. | ||
| IIIA | T2c–d, N0, M0 | –T2c = tamaño tumoral de categoría 2 sin compromiso del cuerpo ciliar, pero con diseminación extraocular que mide ≤5 mm en su diámetro mayor. |
| –T2d = tamaño tumoral de categoría 2 con compromiso del cuerpo ciliar y diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| T3b–c, N0, M0 | –T3b = tamaño tumoral de categoría 3 con compromiso del cuerpo ciliar. | |
| –T3c = tamaño tumoral de categoría 3 sin compromiso del cuerpo ciliar, pero con diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| T4a, N0, M0 | –T4a = tamaño tumoral de categoría 4 sin compromiso del cuerpo ciliar ni diseminación extraocular. | |
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| IIIB | T3d, N0, M0 | –T3d = tamaño tumoral de categoría 3 con compromiso del cuerpo ciliar y diseminación extraocular que mide ≤5 mm en su diámetro mayor. |
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| T4b–c, N0, M0 | –T4b = tamaño tumoral de categoría 4 con compromiso del cuerpo ciliar. | |
| –T4c = tamaño tumoral de categoría 4 sin compromiso del cuerpo ciliar, pero con diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| IIIC | T4d–e, N0, M0 | –T4d = tamaño tumoral de categoría 4 con compromiso del cuerpo ciliar y diseminación extraocular que mide ≤5 mm en su diámetro mayor. |
| –T4e = cualquier categoría de tamaño tumoral con diseminación extraocular que mide >5 mm en su diámetro mayor. | ||
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| Estadio | TNM | Descripción |
|---|---|---|
| T = tumor primario; N = ganglio linfático regional; M = metástasis a distancia. | ||
| a Reproducción autorizada de AJCC: Uveal melanoma. En: Amin, MB, Edge Sb, Greene FL et al., eds.:AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 805–17. | ||
| b 1) Los melanomas primarios de cuerpo ciliar y coroides se clasifican a partir de cuatro categorías de tamaño tumoral según el grosor y el diámetro. Consultar el Cuadro 4. 2) En la práctica clínica, se calcula el diámetro basal mayor del tumor en diámetros de disco óptico (DD; en promedio, 1 DD = 1,5 mm), y el grosor del tumor se calcula en dioptrías (en promedio, 2,5 dioptrías = 1 mm). La ecografía y la fotografía del fondo de ojo se usan para obtener mediciones más exactas. 3) Cuando se registran las mediciones histopatológicas después de la fijación, a veces se subestiman el diámetro y el grosor del tumor debido a la reducción del tejido. | ||
| IV | Cualquier T, N1, M0 | TX = tumor primario no evaluable. |
| T0 = sin indicios de tumor primario. | ||
| T1 = tamaño tumoral de categoría 1. | ||
| –T1a = tamaño tumoral de categoría 1 sin compromiso del cuerpo ciliar ni diseminación extraocular. | ||
| –T1b = tamaño tumoral de categoría 1 con compromiso del cuerpo ciliar. | ||
| –T1c = tamaño tumoral de categoría 1 sin compromiso del cuerpo ciliar, pero con diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| –T1d = tamaño tumoral de categoría 1, con compromiso del cuerpo ciliar y diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| T2 = tamaño tumoral de categoría 2. | ||
| –T2a = tamaño tumoral de categoría 2 sin compromiso del cuerpo ciliar ni diseminación extraocular. | ||
| –T2b = tamaño tumoral de categoría 2 con compromiso del cuerpo ciliar. | ||
| –T2c = tamaño tumoral de categoría 2 sin compromiso del cuerpo ciliar, pero con diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| –T2d = tamaño tumoral de categoría 2 con compromiso del cuerpo ciliar y diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| T3 = tamaño tumoral de categoría 3. | ||
| –T3a = tamaño tumoral de categoría 3 sin compromiso del cuerpo ciliar ni diseminación extraocular. | ||
| –T3b = tamaño tumoral de categoría 3 con compromiso del cuerpo ciliar. | ||
| –T3c = tamaño tumoral de categoría 3 sin compromiso del cuerpo ciliar, pero con diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| –T3d = tamaño tumoral de categoría 3 con compromiso del cuerpo ciliar y diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| T4 = tamaño tumoral de categoría 4. | ||
| –T4a = tamaño tumoral de categoría 4 sin compromiso del cuerpo ciliar ni diseminación extraocular. | ||
| –T4b = tamaño tumoral de categoría 4 con compromiso del cuerpo ciliar. | ||
| –T4c = tamaño tumoral de categoría 4 sin compromiso del cuerpo ciliar, pero con diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| –T4d = tamaño tumoral de categoría 4 con compromiso del cuerpo ciliar y diseminación extraocular que mide ≤5 mm en su diámetro mayor. | ||
| –T4e = cualquier categoría de tamaño tumoral con diseminación extraocular que mide >5 mm en su diámetro mayor. | ||
| N1 = metástasis en ganglios linfáticos regionales o depósitos tumorales separados en la órbita. | ||
| –N1a = metástasis en uno o más ganglios linfáticos regionales. | ||
| –N1b = sin compromiso de ganglios linfáticos regionales, pero con depósitos tumorales separados en la órbita que no son contiguos al ojo. | ||
| M0 = sin metástasis a distancia según la clasificación clínica. | ||
| Cualquier T, cualquier N, M1a–c | Cualquier T = consultar las descripciones más arriba en este cuadro, estadio IV, Cualquier T, N1, M0. | |
| NX = ganglios linfáticos regionales no evaluables. | ||
| N0 = sin compromiso de ganglios linfáticos regionales. | ||
| N1 = metástasis en ganglios linfáticos regionales o depósitos tumorales separados en la órbita. | ||
| –N1a = metástasis en uno o más ganglios linfáticos regionales. | ||
| –N1b = sin compromiso de ganglios linfáticos regionales, pero con depósitos tumorales separados en la órbita que no son contiguos al ojo (coroides y cuerpo ciliar). | ||
| M1 = metástasis a distancia. | ||
| –M1a = el diámetro mayor de la metástasis más grande mide ≤3,0 cm. | ||
| –M1b = el diámetro mayor de la metástasis más grande mide 3,1–8,0 cm. | ||
| –M1c = el diámetro mayor de la metástasis más grande mide ≥8,1 cm. | ||
Características pronósticas
Es importante tomar nota de algunas características pronósticas clave de los melanomas uveales malignos, aunque no se incluyan en los algoritmos de estadificación. Éstas son las siguientes:[
Características moleculares
- Alteraciones cromosómicas.
- Estado del cromosoma 3 (con pérdida o sin pérdida, completa o parcial).
- Estado del cromosoma 6p (con ganancia o sin ganancia).
- Estado del cromosoma 8q (con ganancia o sin ganancia).
Indicar:
- Las técnicas utilizadas para evaluar el estado del cromosoma que incluyen las siguientes.
- Cariotipado.
- Hibridación fluorescente in situ.
- Hibridación genómica comparativa.
- Pérdida de la heterocigosidad en el análisis de polimorfismos del ADN (por ejemplo, polimorfismo mononucleotídicos, microsatélites).
- Otras.
- Los métodos para obtener la muestra que incluyen los siguientes.
- Enucleación.
- Resección local.
- Biopsia.
- Biopsia por aspiración con aguja fina.
- Para las biopsias con aguja, determinar si se hizo una evaluación citopatológica para confirmar la presencia de células tumorales.
- Las técnicas utilizadas para evaluar el estado del cromosoma que incluyen las siguientes.
- Perfil de expresión génica: clase 1 o clase 2.
Indicar:
- La técnica utilizada para determinar el perfil de expresión génica (por ejemplo, micromatriz, respuesta patológica completa).
- Los métodos para obtener la muestra (por ejemplo, enucleación, resección local, biopsia, biopsia por aspiración con aguja fina).
- Para las biopsias con aguja, determinar si se hizo una evaluación citopatológica para confirmar la presencia de células tumorales.
Características clínicas e histopatológicas
- Clínicas.
- Tomografía por emisión de positrones o tomografía computarizada.
- Valores estandarizados de captación de flúor F 18-fludesoxiglucosa (en un tumor primario, los valores más altos a veces se relacionan con una supervivencia más corta).
- Angiografía confocal con verde de indocianina.
- Identificación de configuraciones monocirculatorias complejas (es decir, asas, redes, arcos con ramificaciones, en paralelo con reticulación o una combinación de estos modelos que tal vez se relacionen con una supervivencia más corta).
- Tomografía por emisión de positrones o tomografía computarizada.
- Histopatológicas.
- Recuento mitótico.
- Número de figuras de mitosis por cada 40 campos de gran aumento (área de campo característica de 0,15–0,19 mm2, los recuentos más altos se relacionan con una supervivencia más corta).
- Media del diámetro de los 10 nucléolos más grandes.
- La media de los nucléolos más grandes se mide a lo largo de una franja central de 5 mm; por ejemplo, después de una tinción argéntica (los valores mayores se relacionan con una supervivencia más corta).
- Presencia de configuraciones de matriz extravascular.
- Asas.
- Ausentes.
- Presentes (supervivencia más corta).
- Asas que forman redes.
- Ausentes.
- Presentes (supervivencia más corta).
- Otras configuraciones complejas (ausencia o presencia de arcos con ramificaciones o en paralelo con reticulación).
Las configuraciones se evalúan mediante microscopía óptica con un filtro verde oscuro después de la tinción con ácido peryódico de Schiff sin coloración de contraste.
- Asas.
- Densidad microvascular.
- Número de elementos inmunopositivos con marcación para células endoteliales vasculares (por ejemplo, epítopo CD34, antígeno relacionado con el factor VIII) en las áreas de vascularización más densa (área de campo característica de 0,31 mm2, los recuentos más altos se relacionan con una supervivencia más corta).
- Receptor del factor crecimiento similar a la insulina de tipo 1.
- Porcentaje de células tumorales inmunopositivas (la expresión alta se relaciona con una supervivencia más corta).
- Linfocitos que infiltran el tumor.
- Pocos (supervivencia más larga).
- Cantidad moderada.
- Muchos (supervivencia más corta).
- Macrófagos que infiltran el tumor.
- Pocos (supervivencia más larga).
- Cantidad moderada.
- Muchos (supervivencia más corta).
El número se puede comparar con fotografías estándar.[
12 ]
- Expresión de HLA de clase I.
- Porcentaje de células tumorales inmunopositivas (la expresión baja se relaciona con una supervivencia más larga).
- Recuento mitótico.
Referencias:
- Factors predictive of growth and treatment of small choroidal melanoma: COMS Report No. 5. The Collaborative Ocular Melanoma Study Group. Arch Ophthalmol 115 (12): 1537-44, 1997.
- Diener-West M, Earle JD, Fine SL, et al.: The COMS randomized trial of iodine 125 brachytherapy for choroidal melanoma, II: characteristics of patients enrolled and not enrolled. COMS Report No. 17. Arch Ophthalmol 119 (7): 951-65, 2001.
- Shields CL, Shields JA, De Potter P, et al.: Diffuse choroidal melanoma. Clinical features predictive of metastasis. Arch Ophthalmol 114 (8): 956-63, 1996.
- Scott IU, Murray TG, Hughes JR: Evaluation of imaging techniques for detection of extraocular extension of choroidal melanoma. Arch Ophthalmol 116 (7): 897-9, 1998.
- Romero JM, Finger PT, Iezzi R, et al.: Three-dimensional ultrasonography of choroidal melanoma: extrascleral extension. Am J Ophthalmol 126 (6): 842-4, 1998.
- Echography (ultrasound) procedures for the Collaborative Ocular Melanoma Study (COMS), Report no. 12, Part I. J Ophthalmic Nurs Technol 18 (4): 143-9, 1999 Jul-Aug.
- Uveal melanoma. In: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. Springer; 2017, pp 805–17.
- Dithmar S, Diaz CE, Grossniklaus HE: Intraocular melanoma spread to regional lymph nodes: report of two cases. Retina 20 (1): 76-9, 2000.
- Diener-West M, Reynolds SM, Agugliaro DJ, et al.: Development of metastatic disease after enrollment in the COMS trials for treatment of choroidal melanoma: Collaborative Ocular Melanoma Study Group Report No. 26. Arch Ophthalmol 123 (12): 1639-43, 2005.
- Shields CL, Santos MC, Shields JA, et al.: Extraocular extension of unrecognized choroidal melanoma simulating a primary optic nerve tumor: report of two cases. Ophthalmology 106 (7): 1349-52, 1999.
- Singh AD, Shields JA, Shields CL, et al.: Choroidal melanoma metastatic to the contralateral choroid. Am J Ophthalmol 132 (6): 941-3, 2001.
- Mäkitie T, Summanen P, Tarkkanen A, et al.: Tumor-infiltrating macrophages (CD68(+) cells) and prognosis in malignant uveal melanoma. Invest Ophthalmol Vis Sci 42 (7): 1414-21, 2001.
Aspectos generales de las opciones de tratamiento
Función de la observación
Los melanomas de iris tienen desenlaces relativamente buenos con una tasa de supervivencia a 5 años de más del 95 %. En su mayoría se componen de células fusiformes y a menudo su tamaño es más pequeño que los melanomas posteriores porque se detectan más rápido. En general, se prefiere un tratamiento conservador cuando sea posible, pero a veces se justifica una intervención quirúrgica cuando el crecimiento tumoral es evidente o la enfermedad está diseminada en el momento del examen inicial.
El abordaje terapéutico de los melanomas de coroides pequeños es polémico y no está claro si el tratamiento de los tumores pequeños previene la metástasis.[
Aunque los pacientes con diagnóstico de tumores de coroides pequeños no fueron aptos para participar en el Collaborative Ocular Melanoma Study (COMS), se les ofreció participar en un estudio prospectivo de seguimiento para evaluar la evolución natural de lesiones pequeñas. Se notificaron cálculos de crecimiento tumoral a 2 años del 21 % y de crecimiento tumoral a 5 años del 31 %.[
- Aumento del grosor del tumor.
- Líquido subretiniano.
- Pigmentación anaranjada.
- Ausencia de drusas.
- Ausencia de pigmento en la retina.
- Margen en el disco óptico.
- Cambios epiteliales alrededor del tumor.
Función de la cirugía
La selección del tratamiento depende de los siguientes aspectos:
- Sitio de origen (coroides, cuerpo ciliar, iris).
- Tamaño y localización de la lesión.
- Edad del paciente.
- Invasión extraocular, recidiva o metástasis.
Enucleación
En el pasado, la enucleación (extirpación del ojo) fue el tratamiento estándar para el melanoma primario de coroides y todavía se usa para tumores grandes. Sin embargo, para preservar el ojo afectado ahora se usa más la radioterapia (es decir, braquiterapia con placas radiactivas o radioterapia de haz externo con partículas cargadas) en lugar de la enucleación.[
Radioterapia de haz externo antes de la enucleación
En un ensayo aleatorizado se probó la función de la administración de radioterapia de haz externo (RHE) antes de la enucleación para los pacientes con tumores de coroides grandes en quienes la enucleación se considera necesaria y no se observó un efecto en la supervivencia general (SG).[
Resección transescleral local
La resección transescleral local para preservar el ojo tiene una función limitada en el tratamiento del melanoma uveal. Se usa para pacientes con tumores grandes de coroides y cuerpo ciliar que no son aptos para recibir radioterapia, pero que tienen gran interés en conservar su ojo.[
Resección quirúrgica de las metástasis
Se notificó la resección quirúrgica de las metástasis de melanoma ocular en series de casos de pacientes muy selectos que en ocasiones tuvieron desenlaces favorables.[
Función de la radioterapia
La braquiterapia epiescleral con placas que contienen semillas radiactivas pequeñas es la forma más común de radiación para el tratamiento del melanoma ocular. El yodo I 125 (125I), el cobalto Co 60 (60Co), el paladio Pd 103 (103Pd), el iridio Ir 192 (192Ir) y el rutenio Ru 106 (106Ru) son ejemplos de isótopos radiactivos que se usan para la braquiterapia con placas. Es más fácil blindar contra los isótopos que tienen emisiones relativamente bajas de fotones y electrones (125I, 103Pd y 106Ru) con el fin de reducir la exposición de los tejidos adyacentes normales, y es probable que 125I sea el radioisótopo de mayor uso.[
En una serie de casos con 1106 pacientes de melanoma uveal tratados con radioterapia con placa, que tenían al inicio una agudeza visual de por lo menos 20/100, el 68 % presentaron agudeza visual precaria (es decir, 20/200 o peor) en el transcurso de 10 años.[
Los factores relacionados con los resultados de agudeza visual más desfavorables fueron los siguientes:[
- Edad mayor de 60 años.
- Agudeza visual precaria al inicio.
- Diabetes.
- Aumento del tamaño y grosor del tumor.
- Localización cerca de la fóvea o el disco óptico.
- Uso de isótopos (106Ru, 60Co o 192Ir vs. 125I).
La braquiterapia con 125I y la enucleación tienen tasas equivalentes de supervivencia general y específica de melanoma metastásico cuando se usan para melanomas de tamaño mediano.[
En un estudio complementario dentro del COMS, a 209 pacientes se les hizo una evaluación prospectiva de la calidad de vida durante los 5 primeros años de seguimiento.[
La RHE con partículas cargadas (usando protones, iones de carbono o de helio) es una de las principales formas de radioterapia para el tratamiento de los melanomas oculares.[
En un estudio de un centro con un solo cirujano, se asignó al azar a 184 pacientes con melanomas uveales de menos de 15 mm de diámetro y menos de 10 mm de grosor a recibir braquiterapia con 125I o radiación con iones de helio (en dosis calculadas equivalentes de 70 Gy administradas en 5 fracciones durante 7 a 11 días en cada grupo).[
Debido a la distribución de las dosis, la irradiación con partículas cargadas es más eficaz que la braquiterapia con placa para tratar tumores más grandes y que están más cerca de la fóvea o el disco óptico. En una serie numerosa de un centro único con un solo cirujano, 2069 pacientes que recibieron terapia de haz de protones tuvieron una tasa actuarial de control local del 95 % (IC 95 %, 93–96 %) a los 15 años. La tasa acumulada de enucleación fue del 16 % (IC 95 %, 13–20 %), a menudo debido a un glaucoma neovascular en el 46 % de las enucleaciones, molestias oculares y ceguera en el 31 % de las enucleaciones, o recidiva local en el 23 % de las enucleaciones. Del mismo modo que para la radiación con placa, los factores de riesgo de deterioro de la agudeza visual después de la radiación con partículas cargadas fueron el tamaño del tumor, la localización cercana a la fóvea o el disco óptico, la agudeza visual al inicio y una diabetes subyacente.[
De la misma manera, en otro estudio de un solo centro con un solo cirujano de una serie consecutiva con 886 pacientes tratados con irradiación con haz de protones, se notificó una tasa de control local del 92,1 % (IC 95 %, 89,8–94,6 %) y una tasa de preservación ocular a los 10 años dl 87,3 % (IC 95 %, 83,9–90,9 %).[
En un estudio de fase I/II de un solo centro con 57 pacientes evaluables que recibieron irradiación con haz de iones de carbono y se sometieron a seguimiento durante una mediana de 26 meses, se encontró que 26 pacientes presentaron glaucoma neurovascular o dolor ocular intenso debido al aumento de la presión intraocular y 3 pacientes se sometieron a enucleación. Un paciente presentó recidiva tumoral local.[
Con el fin de disminuir la tasa de complicaciones y mejorar el resultado funcional, se compararon dosis reducidas de 50 Gy equivalentes de cobalto (CGE) con un haz de protones de 70 CGE (cada dosis administrada en 5 fracciones, por lo general en un período de 7 días). Los pacientes (n = 188) con tumores que medían menos de 15 mm de diámetro y menos de 5 mm de altura localizados cerca del disco óptico o la mácula, se asignaron al azar a una de las dos dosis en el marco de un estudio diseñado con enmascaramiento doble. A los 5 años, no hubo diferencias estadísticamente significativas de control tumoral local, tasas de metástasis, agudeza visual o tasas de complicaciones. Sin embargo, los campos visuales fueron mejores en el grupo de 50 CGE.[
Como se indicó antes en la sección Función de la cirugía, se probó la función de la radioterapia externa con haz fotones antes de la enucleación en un ensayo aleatorizado y no se observó un efecto en la SG de pacientes con tumores de coroides grandes tratados con enucleación.[
Se estudia la radioterapia externa con haz de fotones (rayos γ) combinada con radiocirugía estereotáctica con bisturí de rayos γ como radiación de fracción única [
Función de la termoterapia transpupilar
Para la termoterapia transpupilar (TTT) se dirige un láser infrarrojo, a menudo de 810 nm de longitud de onda, a través de una pupila dilatada durante una o más sesiones con el fin de producir necrosis por calor en los melanomas uveales. Este método conlleva la ventaja teórica de que se destruye el tejido tumoral con alta precisión bajo visualización directa. No obstante, la TTT tiene limitaciones importantes que restringe su uso a circunstancias específicas.[
En un estudio de un solo centro, 95 pacientes con melanomas de coroides pequeños (diámetro <10 mm y grosor <3,5 mm) se asignaron al azar para recibir TTT o braquiterapia con 125I (100 Gy).[
La TTT también está en evaluación como complemento del tratamiento primario de radiación con haz de protones. En el entorno de melanomas uveales grandes, la terapia con haz de protones se relaciona con complicaciones exudativas, inflamatorias y glaucomatosas que a veces exigen enucleación. En un ensayo de un centro único, 151 pacientes con melanomas uveales de por lo menos 7 mm de grosor o por lo menos 15 mm de diámetro se asignaron al azar para recibir radiación con haz de protones (60 CGE en 4 fracciones diarias) con TTT (longitud de onda de 810 nm al cabo de 1, 6 y 12 meses del tratamiento) o sin esta y se los siguió durante una mediana de 38 meses.[
Hay incertidumbre con respecto al tratamiento óptimo del melanoma ocular. Los médicos deben mencionar las oportunidades de participar en ensayos clínicos a los pacientes aptos. Para obtener información sobre los ensayos clínicos en curso, consultar el
Referencias:
- Shields CL, Shields JA, Perez N, et al.: Primary transpupillary thermotherapy for small choroidal melanoma in 256 consecutive cases: outcomes and limitations. Ophthalmology 109 (2): 225-34, 2002.
- Augsburger JJ: Is observation really appropriate for small choroidal melanomas. Trans Am Ophthalmol Soc 91: 147-68; discussion 169-75, 1993.
- Shields CL, Cater J, Shields JA, et al.: Combination of clinical factors predictive of growth of small choroidal melanocytic tumors. Arch Ophthalmol 118 (3): 360-4, 2000.
- Robertson DM, Buettner H, Bennett SR: Transpupillary thermotherapy as primary treatment for small choroidal melanomas. Arch Ophthalmol 117 (11): 1512-9, 1999.
- Factors predictive of growth and treatment of small choroidal melanoma: COMS Report No. 5. The Collaborative Ocular Melanoma Study Group. Arch Ophthalmol 115 (12): 1537-44, 1997.
- Zimmerman LE, McLean IW, Foster WD: Statistical analysis of follow-up data concerning uveal melanomas, and the influence of enucleation. Ophthalmology 87 (6): 557-64, 1980.
- De Potter P, Shields CL, Shields JA: New treatment modalities for uveal melanoma. Curr Opin Ophthalmol 7 (3): 27-32, 1996.
- The Collaborative Ocular Melanoma Study (COMS) randomized trial of pre-enucleation radiation of large choroidal melanoma II: initial mortality findings. COMS report no. 10. Am J Ophthalmol 125 (6): 779-96, 1998.
- Hawkins BS; Collaborative Ocular Melanoma Study Group: The Collaborative Ocular Melanoma Study (COMS) randomized trial of pre-enucleation radiation of large choroidal melanoma: IV. Ten-year mortality findings and prognostic factors. COMS report number 24. Am J Ophthalmol 138 (6): 936-51, 2004.
- Damato B: The role of eyewall resection in uveal melanoma management. Int Ophthalmol Clin 46 (1): 81-93, 2006.
- Bechrakis NE, Bornfeld N, Zöller I, et al.: Iodine 125 plaque brachytherapy versus transscleral tumor resection in the treatment of large uveal melanomas. Ophthalmology 109 (10): 1855-61, 2002.
- Bechrakis NE, Petousis V, Willerding G, et al.: Ten-year results of transscleral resection of large uveal melanomas: local tumour control and metastatic rate. Br J Ophthalmol 94 (4): 460-6, 2010.
- Hsueh EC, Essner R, Foshag LJ, et al.: Prolonged survival after complete resection of metastases from intraocular melanoma. Cancer 100 (1): 122-9, 2004.
- Pawlik TM, Zorzi D, Abdalla EK, et al.: Hepatic resection for metastatic melanoma: distinct patterns of recurrence and prognosis for ocular versus cutaneous disease. Ann Surg Oncol 13 (5): 712-20, 2006.
- Albert DM, Kulkarni AD: Intraocular melanoma. In: DeVita VT Jr, Lawrence TS, Rosenberg SA: Cancer: Principles and Practice of Oncology. 9th ed. Lippincott Williams & Wilkins, 2011, pp 2090-8.
- Shields CL, Shields JA, Cater J, et al.: Plaque radiotherapy for uveal melanoma: long-term visual outcome in 1106 consecutive patients. Arch Ophthalmol 118 (9): 1219-28, 2000.
- Diener-West M, Earle JD, Fine SL, et al.: The COMS randomized trial of iodine 125 brachytherapy for choroidal melanoma, III: initial mortality findings. COMS Report No. 18. Arch Ophthalmol 119 (7): 969-82, 2001.
- Collaborative Ocular Melanoma Study Group: The COMS randomized trial of iodine 125 brachytherapy for choroidal melanoma: V. Twelve-year mortality rates and prognostic factors: COMS report No. 28. Arch Ophthalmol 124 (12): 1684-93, 2006.
- Melia M, Moy CS, Reynolds SM, et al.: Quality of life after iodine 125 brachytherapy vs enucleation for choroidal melanoma: 5-year results from the Collaborative Ocular Melanoma Study: COMS QOLS Report No. 3. Arch Ophthalmol 124 (2): 226-38, 2006.
- Char DH, Kroll S, Phillips TL, et al.: Late radiation failures after iodine 125 brachytherapy for uveal melanoma compared with charged-particle (proton or helium ion) therapy. Ophthalmology 109 (10): 1850-4, 2002.
- Gragoudas E, Li W, Goitein M, et al.: Evidence-based estimates of outcome in patients irradiated for intraocular melanoma. Arch Ophthalmol 120 (12): 1665-71, 2002.
- Caujolle JP, Mammar H, Chamorey E, et al.: Proton beam radiotherapy for uveal melanomas at nice teaching hospital: 16 years' experience. Int J Radiat Oncol Biol Phys 78 (1): 98-103, 2010.
- Tsuji H, Ishikawa H, Yanagi T, et al.: Carbon-ion radiotherapy for locally advanced or unfavorably located choroidal melanoma: a Phase I/II dose-escalation study. Int J Radiat Oncol Biol Phys 67 (3): 857-62, 2007.
- Char DH, Quivey JM, Castro JR, et al.: Helium ions versus iodine 125 brachytherapy in the management of uveal melanoma. A prospective, randomized, dynamically balanced trial. Ophthalmology 100 (10): 1547-54, 1993.
- Gragoudas ES, Lane AM, Regan S, et al.: A randomized controlled trial of varying radiation doses in the treatment of choroidal melanoma. Arch Ophthalmol 118 (6): 773-8, 2000.
- Modorati G, Miserocchi E, Galli L, et al.: Gamma knife radiosurgery for uveal melanoma: 12 years of experience. Br J Ophthalmol 93 (1): 40-4, 2009.
- Muller K, Nowak PJ, de Pan C, et al.: Effectiveness of fractionated stereotactic radiotherapy for uveal melanoma. Int J Radiat Oncol Biol Phys 63 (1): 116-22, 2005.
- Dieckmann K, Georg D, Bogner J, et al.: Optimizing LINAC-based stereotactic radiotherapy of uveal melanomas: 7 years' clinical experience. Int J Radiat Oncol Biol Phys 66 (4 Suppl 1): 47-52, 2006.
- Harbour JW, Meredith TA, Thompson PA, et al.: Transpupillary thermotherapy versus plaque radiotherapy for suspected choroidal melanomas. Ophthalmology 110 (11): 2207-14; discussion 2215, 2003.
- Pilotto E, Vujosevic S, De Belvis V, et al.: Long-term choroidal vascular changes after iodine brachytherapy versus transpupillary thermotherapy for choroidal melanoma. Eur J Ophthalmol 19 (4): 646-53, 2009 Jul-Aug.
- Desjardins L, Lumbroso-Le Rouic L, Levy-Gabriel C, et al.: Combined proton beam radiotherapy and transpupillary thermotherapy for large uveal melanomas: a randomized study of 151 patients. Ophthalmic Res 38 (5): 255-60, 2006.
Tratamiento del melanoma de iris
Las proliferaciones melanocíticas estromales y los nevos de iris son los tumores de iris más comunes, aunque el melanoma es poco frecuente.[
La evaluación periódica de los melanomas de iris incluye gonioscopía, transiluminación del globo ocular y oftalmoscopia indirecta con 360° de depresión escleral. Es esencial documentar con fotografías para registrar la progresión de tamaño o crecimiento del tumor.[
En general, los pacientes con melanomas de iris tienen desenlaces relativamente buenos. Solo cerca del 3 % de estos melanomas metastatizan en el transcurso de 5 años.[
Dada la poca frecuencia de los melanomas de iris y su buen pronóstico, no es posible hacer ensayos clínicos con suficiente potencia estadística. Pero, la experiencia de tratamiento se basa principalmente en series e informes de casos. En general se prefiere un tratamiento conservador cuando sea posible, pero a veces se justifica una intervención quirúrgica cuando el crecimiento tumoral es evidente o la enfermedad está diseminada en el momento del examen inicial.
Opciones de tratamiento del melanoma de iris
Las opciones de tratamiento del melanoma de iris son las siguientes:
- Observación con seguimiento atento. Esta opción se emplea para los pacientes asintomáticos que tienen lesiones estables; el seguimiento incluye fotografías seriadas.[
3 ] - Resección local. Esta opción se emplea cuando se registra crecimiento progresivo y pronunciado.[
2 ] - Enucleación. Esta opción se emplea cuando el tumor no se puede tratar con resección local debido a compromiso difuso del iris, compromiso de más del 50 % del iris y el ángulo de la cámara anterior, glaucoma intratable o diseminación extraocular.[
7 ] - Radioterapia con placa. Esta opción se ofrece como una alternativa para las lesiones grandes y difusas ubicadas en el iris y que no se pueden resecar con cirugía.[
8 ]
Ensayos clínicos en curso
Realizar una
Referencias:
- Albert DM, Kulkarni AD: Intraocular melanoma. In: DeVita VT Jr, Lawrence TS, Rosenberg SA: Cancer: Principles and Practice of Oncology. 9th ed. Lippincott Williams & Wilkins, 2011, pp 2090-8.
- Starr OD, Patel DV, Allen JP, et al.: Iris melanoma: pathology, prognosis and surgical intervention. Clin Experiment Ophthalmol 32 (3): 294-6, 2004.
- Marcus DM, Sahel JA, Jakobiec FA, et al.: Pigmented tumors of the iris. In: Albert DM, Jakobiec FA, eds.: Principles and Practice of Ophthalmology. WB Saunders Co., 1994, pp 3198-3208.
- Yap-Veloso MI, Simmons RB, Simmons RJ: Iris melanomas: diagnosis and management. Int Ophthalmol Clin 37 (4): 87-100, 1997 Fall.
- Pavlin CJ, McWhae JA, McGowan HD, et al.: Ultrasound biomicroscopy of anterior segment tumors. Ophthalmology 99 (8): 1220-8, 1992.
- Conway RM, Chua WC, Qureshi C, et al.: Primary iris melanoma: diagnostic features and outcome of conservative surgical treatment. Br J Ophthalmol 85 (7): 848-54, 2001.
- Melanocytic tumors of the iris stroma. In: Shields JA: Diagnosis and Management of Intraocular Tumors. C.V. Mosby Company, 1983, pp 83-121.
- Shields CL, Shields JA, De Potter P, et al.: Treatment of non-resectable malignant iris tumours with custom designed plaque radiotherapy. Br J Ophthalmol 79 (4): 306-12, 1995.
Tratamiento del melanoma de cuerpo ciliar
El melanoma que compromete el cuerpo ciliar es un tumor poco frecuente con pronóstico precario. En algunos casos, el diagnóstico es difícil debido a la similitud con otras enfermedades oculares. Se debe considerar el melanoma de cuerpo ciliar durante el diagnóstico diferencial para casos de glaucoma pigmentario unilateral y uveítis crónica.[
La biomicroscopia ecográfica se puede usar para evaluar la forma, el grosor, los márgenes, la reflectividad y la invasión local del tumor.[
Opciones de tratamiento del melanoma de cuerpo ciliar
Hay varias opciones de tratamiento del melanoma de cuerpo ciliar. Todas se notificaron en series de casos.[Nivel de evidencia C3] No obstante, la elección del tratamiento depende de muchos factores.
Las opciones de tratamiento del melanoma de cuerpo ciliar son las siguientes:
- Radioterapia con placa. Las tasas de control local son altas, pero el tratamiento se relaciona con una incidencia alta de catarata secundaria.[
4 ,5 ] - Radioterapia externa con partículas cargadas. Este abordaje se ofrece en centros de referencia especializados. Exige la cooperación atenta del paciente para fijar la mirada de manera voluntaria.[
6 ,7 ,8 ] - Resección tumoral local. Esta opción es adecuada principalmente para tumores de cuerpo ciliar o de coroides anterior seleccionados por sus dimensiones basales más pequeñas y mayor grosor.[
9 ,10 ] - Enucleación. Esta opción se reserva por lo general para melanomas grandes cuando no quedan esperanzas de recuperar la vista útil. También se indica cuando hay un glaucoma secundario resistente al tratamiento y diseminación extraocular.[
5 ,8 ]
Ensayos clínicos en curso
Realizar una
Referencias:
- Nguyen QD, Foster CS: Ciliary body melanoma masquerading as chronic uveitis. Ocul Immunol Inflamm 6 (4): 253-6, 1998.
- Marigo FA, Finger PT, McCormick SA, et al.: Iris and ciliary body melanomas: ultrasound biomicroscopy with histopathologic correlation. Arch Ophthalmol 118 (11): 1515-21, 2000.
- Daftari I, Barash D, Lin S, et al.: Use of high-frequency ultrasound imaging to improve delineation of anterior uveal melanoma for proton irradiation. Phys Med Biol 46 (2): 579-90, 2001.
- Gündüz K, Shields CL, Shields JA, et al.: Plaque radiotherapy of uveal melanoma with predominant ciliary body involvement. Arch Ophthalmol 117 (2): 170-7, 1999.
- Finger PT: Plaque radiation therapy for malignant melanoma of the iris and ciliary body. Am J Ophthalmol 132 (3): 328-35, 2001.
- Munzenrider JE: Uveal melanomas. Conservation treatment. Hematol Oncol Clin North Am 15 (2): 389-402, 2001.
- Char DH, Kroll SM, Castro J: Ten-year follow-up of helium ion therapy for uveal melanoma. Am J Ophthalmol 125 (1): 81-9, 1998.
- De Potter P: [Choroidal melanoma: current therapeutic approaches] J Fr Ophtalmol 25 (2): 203-11, 2002.
- De Potter P, Shields CL, Shields JA: New treatment modalities for uveal melanoma. Curr Opin Ophthalmol 7 (3): 27-32, 1996.
- Char DH, Miller T, Crawford JB: Uveal tumour resection. Br J Ophthalmol 85 (10): 1213-9, 2001.
Tratamiento del melanoma de coroides pequeño
En los pacientes tratados por melanomas de coroides pequeños se notificó un intervalo amplio de tasas de mortalidad a 5 años, la tasa promedio es de cerca del 16 %.[
El tratamiento de los melanomas de coroides pequeños es polémico. No se ha descrito bien la probabilidad de progresión desde el momento del diagnóstico hasta el crecimiento que justifique iniciar un tratamiento. Muchos oftalmólogos recomiendan la observación inicial. Esta estrategia de tratamiento inicial se justifica por distintas razones, entre ellas, la dificultad para establecer un diagnóstico correcto, la ausencia de eficacia documentada para los tratamientos que preservan el globo ocular y las preocupaciones por la morbilidad grave relacionada con el tratamiento. Otros promueven la intervención terapéutica más temprana.[
Opciones de tratamiento del melanoma de coroides pequeño
Las opciones de tratamiento del melanoma de coroides pequeño son las siguientes:
- Observación. Esta estrategia es importante para los pacientes con diagnóstico incierto o sin crecimiento del tumor registrado. También se usa para pacientes asintomáticos con lesiones estables (en particular, pacientes mayores o debilitados) y pacientes con un tumor en el único ojo útil.[
2 ] - Radioterapia con placa. Este tratamiento se utiliza para melanomas uveales de tamaño pequeño o mediano, tumores amelanóticos o tumores en contacto con el disco óptico en un área que mide más de tres horas de la circunferencia del disco óptico.[
7 ,8 ] - Radioterapia externa con partículas cargadas. Este abordaje se ofrece en centros de referencia especializados. Exige la cooperación atenta del paciente para fijar la mirada de manera voluntaria.[
7 ,8 ,9 ,10 ] - Radiocirugía con bisturí de rayos γ. Este tratamiento quizás sea una opción viable para melanomas pequeños y medianos.[
11 ,12 ,13 ] - Termoterapia transpupilar. Como se mencionó antes, este abordaje tiene un uso muy limitado, pero a veces se emplea como tratamiento primario o complementario de la radioterapia con placa.[
5 ,6 ,14 ,15 ,16 ,17 ,18 ] Para obtener más información, consultar la sección Función de la termoterapia transpupilar. - Resección tumoral local. Esta estrategia se utiliza principalmente para tumores de cuerpo ciliar o de coroides anterior seleccionados por sus dimensiones basales más pequeñas y mayor grosor.[
19 ] - Enucleación. Este abordaje se utiliza cuando hay elevación grave de la presión ocular. También se puede considerar para melanomas de tamaño pequeño y mediano que invaden los tejidos del nervio óptico.[
20 ]
Ensayos clínicos en curso
Realizar una
Referencias:
- Diener-West M, Hawkins BS, Markowitz JA, et al.: A review of mortality from choroidal melanoma. II. A meta-analysis of 5-year mortality rates following enucleation, 1966 through 1988. Arch Ophthalmol 110 (2): 245-50, 1992.
- Mortality in patients with small choroidal melanoma. COMS report no. 4. The Collaborative Ocular Melanoma Study Group. Arch Ophthalmol 115 (7): 886-93, 1997.
- Shields CL, Shields JA, Kiratli H, et al.: Risk factors for growth and metastasis of small choroidal melanocytic lesions. Ophthalmology 102 (9): 1351-61, 1995.
- Shields CL, Cater J, Shields JA, et al.: Combination of clinical factors predictive of growth of small choroidal melanocytic tumors. Arch Ophthalmol 118 (3): 360-4, 2000.
- Shields CL, Shields JA, Perez N, et al.: Primary transpupillary thermotherapy for small choroidal melanoma in 256 consecutive cases: outcomes and limitations. Ophthalmology 109 (2): 225-34, 2002.
- Robertson DM, Buettner H, Bennett SR: Transpupillary thermotherapy as primary treatment for small choroidal melanomas. Arch Ophthalmol 117 (11): 1512-9, 1999.
- Shields CL, Shields JA, Gündüz K, et al.: Radiation therapy for uveal malignant melanoma. Ophthalmic Surg Lasers 29 (5): 397-409, 1998.
- Finger PT: Radiation therapy for choroidal melanoma. Surv Ophthalmol 42 (3): 215-32, 1997 Nov-Dec.
- Munzenrider JE: Uveal melanomas. Conservation treatment. Hematol Oncol Clin North Am 15 (2): 389-402, 2001.
- Char DH, Kroll SM, Castro J: Ten-year follow-up of helium ion therapy for uveal melanoma. Am J Ophthalmol 125 (1): 81-9, 1998.
- Woodburn R, Danis R, Timmerman R, et al.: Preliminary experience in the treatment of choroidal melanoma with gamma knife radiosurgery. J Neurosurg 93 (Suppl 3): 177-9, 2000.
- Modorati G, Miserocchi E, Galli L, et al.: Gamma knife radiosurgery for uveal melanoma: 12 years of experience. Br J Ophthalmol 93 (1): 40-4, 2009.
- Muller K, Nowak PJ, de Pan C, et al.: Effectiveness of fractionated stereotactic radiotherapy for uveal melanoma. Int J Radiat Oncol Biol Phys 63 (1): 116-22, 2005.
- Shields CL, Shields JA: Transpupillary thermotherapy for choroidal melanoma. Curr Opin Ophthalmol 10 (3): 197-203, 1999.
- Godfrey DG, Waldron RG, Capone A: Transpupillary thermotherapy for small choroidal melanoma. Am J Ophthalmol 128 (1): 88-93, 1999.
- Bartlema YM, Oosterhuis JA, Journée-De Korver JG, et al.: Combined plaque radiotherapy and transpupillary thermotherapy in choroidal melanoma: 5 years' experience. Br J Ophthalmol 87 (11): 1370-3, 2003.
- Harbour JW, Meredith TA, Thompson PA, et al.: Transpupillary thermotherapy versus plaque radiotherapy for suspected choroidal melanomas. Ophthalmology 110 (11): 2207-14; discussion 2215, 2003.
- Pilotto E, Vujosevic S, De Belvis V, et al.: Long-term choroidal vascular changes after iodine brachytherapy versus transpupillary thermotherapy for choroidal melanoma. Eur J Ophthalmol 19 (4): 646-53, 2009 Jul-Aug.
- Char DH, Miller T, Crawford JB: Uveal tumour resection. Br J Ophthalmol 85 (10): 1213-9, 2001.
- Shields JA, Shields CL: Atlas of Intraocular Tumors. Lippincott Williams & Wilkins, 1999.
Tratamiento del melanoma de coroides mediano y grande
La radioterapia para preservar el ojo, acompañada de braquiterapia con placas o de haz externo, es la opción preferida para la mayoría de los pacientes con melanoma de coroides de tamaño mediano. La enucleación aún es la terapia estándar para la mayoría de los melanomas de coroides grandes y los melanomas que causan glaucoma grave o invaden el nervio óptico.
Opciones de tratamiento para el melanoma de coroides mediano y grande
La configuración del crecimiento tumoral es un factor en la decisión terapéutica. Si hay un melanoma difuso o diseminación extraocular, se debe considerar la enucleación, pero se puede usar radioterapia para una enfermedad menos diseminada.
Las opciones de tratamiento del melanoma de coroides mediano y grande son las siguientes:
Melanomas de coroides medianos
- Radioterapia con placa.[
1 ,2 ,3 ,4 ] - Radioterapia externa con partículas cargadas. Este abordaje se ofrece en centros de referencia especializados. Exige la cooperación atenta del paciente para fijar la mirada de manera voluntaria.[
5 ,6 ,7 ] - Resección local de la pared ocular.[
8 ,9 ] - Terapia combinada, con coagulación de láser ablativo o termoterapia transpupilar para complementar el tratamiento con placa.[
10 ,11 ] Para obtener más información, consultar la sección Función de la termoterapia transpupilar. - Enucleación. Este abordaje se considera principalmente para melanomas difusos o casos que tienen diseminación extraocular. Las complicaciones de la radiación o la recidiva tumoral en ocasiones hacen que la enucleación sea imprescindible.[
10 ]
Melanomas de coroides grandes
- Enucleación cuando se considera que el tumor es demasiado grande como para utilizar abordajes para preservar el ojo.
Ensayos clínicos en curso
Realizar una
Referencias:
- Karvat A, Duzenli C, Ma R, et al.: The treatment of choroidal melanoma with 198 Au plaque brachytherapy. Radiother Oncol 59 (2): 153-6, 2001.
- Tabandeh H, Chaudhry NA, Murray TG, et al.: Intraoperative echographic localization of iodine-125 episcleral plaque for brachytherapy of choroidal melanoma. Am J Ophthalmol 129 (2): 199-204, 2000.
- Diener-West M, Earle JD, Fine SL, et al.: The COMS randomized trial of iodine 125 brachytherapy for choroidal melanoma, III: initial mortality findings. COMS Report No. 18. Arch Ophthalmol 119 (7): 969-82, 2001.
- Melia BM, Abramson DH, Albert DM, et al.: Collaborative ocular melanoma study (COMS) randomized trial of I-125 brachytherapy for medium choroidal melanoma. I. Visual acuity after 3 years COMS report no. 16. Ophthalmology 108 (2): 348-66, 2001.
- Char DH, Quivey JM, Castro JR, et al.: Helium ions versus iodine 125 brachytherapy in the management of uveal melanoma. A prospective, randomized, dynamically balanced trial. Ophthalmology 100 (10): 1547-54, 1993.
- Fuss M, Loredo LN, Blacharski PA, et al.: Proton radiation therapy for medium and large choroidal melanoma: preservation of the eye and its functionality. Int J Radiat Oncol Biol Phys 49 (4): 1053-9, 2001.
- Char DH, Kroll SM, Castro J: Ten-year follow-up of helium ion therapy for uveal melanoma. Am J Ophthalmol 125 (1): 81-9, 1998.
- Char DH, Miller T, Crawford JB: Uveal tumour resection. Br J Ophthalmol 85 (10): 1213-9, 2001.
- Peyman GA, Juarez CP, Diamond JG, et al.: Ten years experience with eye wall resection for uveal malignant melanomas. Ophthalmology 91 (12): 1720-5, 1984.
- Seregard S, Landau I: Transpupillary thermotherapy as an adjunct to ruthenium plaque radiotherapy for choroidal melanoma. Acta Ophthalmol Scand 79 (1): 19-22, 2001.
- Shields JA: The expanding role of laser photocoagulation for intraocular tumors. The 1993 H. Christian Zweng Memorial Lecture. Retina 14 (4): 310-22, 1994.
Tratamiento de la diseminación extraocular y el melanoma ocular metastásico
La diseminación extraescleral confiere un pronóstico precario. Para pacientes con compromiso tumoral macroscópico de la órbita, el tratamiento exige la exenteración orbitaria. No obstante, no hay datos probatorios que indiquen que esta cirugía radical prolongue la vida. La mayoría de los pacientes con diseminación extraocular localizada o encapsulada no se someten a exenteración. Este es un tema polémico.[
No se ha identificado un método eficaz de tratamiento sistémico para pacientes con melanoma ocular metastásico. La participación en ensayos clínicos es una opción para estos pacientes.
Ensayos clínicos en curso
Realizar una
Referencias:
- Shammas HF, Blodi FC: Prognostic factors in choroidal and ciliary body melanomas. Arch Ophthalmol 95 (1): 63-9, 1977.
- Pach JM, Robertson DM, Taney BS, et al.: Prognostic factors in choroidal and ciliary body melanomas with extrascleral extension. Am J Ophthalmol 101 (3): 325-31, 1986.
- Kersten RC, Tse DT, Anderson RL, et al.: The role of orbital exenteration in choroidal melanoma with extrascleral extension. Ophthalmology 92 (3): 436-43, 1985.
- Hykin PG, McCartney AC, Plowman PN, et al.: Postenucleation orbital radiotherapy for the treatment of malignant melanoma of the choroid with extrascleral extension. Br J Ophthalmol 74 (1): 36-9, 1990.
- Gündüz K, Shields CL, Shields JA, et al.: Plaque radiotherapy for management of ciliary body and choroidal melanoma with extraocular extension. Am J Ophthalmol 130 (1): 97-102, 2000.
Tratamiento del melanoma ocular recidivante
El pronóstico para cualquier paciente con enfermedad recidivante o con recaída es precario, sin importar el tipo de célula o el estadio. La decisión de administrar tratamiento adicional y la selección del mismo dependen de muchos factores, entre ellos, el grado de la lesión, la edad y la salud del paciente, el tratamiento previo y el sitio de recidiva, así como consideraciones individuales del paciente. En una serie de casos de un solo centro con pacientes muy seleccionados, se notificó la resección quirúrgica de metástasis diagnosticadas después del tratamiento inicial de un melanoma ocular. No queda claro en qué medida los desenlaces favorables ocasionales son consecuencia de factores de selección firmes, por lo tanto, este abordaje no se puede considerar estándar.[
Siempre que sea posible, se debe aconsejar la participación en ensayos clínicos para los pacientes aptos.
Ensayos clínicos en curso
Realizar una
Referencias:
- Hsueh EC, Essner R, Foshag LJ, et al.: Prolonged survival after complete resection of metastases from intraocular melanoma. Cancer 100 (1): 122-9, 2004.
Actualizaciones más recientes a este resumen (08 / 18 / 2023)
Los resúmenes del PDQ con información sobre el cáncer se revisan con regularidad y se actualizan a medida que se obtiene nueva información. Esta sección describe los cambios más recientes introducidos a este resumen a partir de la fecha arriba indicada.
Se incorporaron cambios editoriales en este resumen.
El
Información sobre este resumen del PDQ
Propósito de este resumen
Este resumen de información del PDQ sobre el cáncer dirigido a profesionales de la salud proporciona información integral revisada por expertos y basada en la evidencia sobre el tratamiento del melanoma ocular uveal. El objetivo es servir como fuente de información y ayuda para los profesionales clínicos durante la atención de pacientes. No ofrece pautas ni recomendaciones formales para tomar decisiones relacionadas con la atención sanitaria.
Revisores y actualizaciones
El
Cada mes, los integrantes de este consejo revisan los artículos publicados recientemente para determinar lo siguiente:
- Si el artículo se debe analizar en una reunión del consejo.
- Si conviene añadir texto acerca del artículo.
- Si se debe reemplazar o actualizar un artículo que ya se citó.
Los cambios en los resúmenes se deciden mediante consenso de los integrantes del consejo después de evaluar la solidez de la evidencia de los artículos publicados y determinar la forma de incorporar el artículo en el resumen.
Cualquier comentario o pregunta sobre el contenido de este resumen se debe enviar al
Niveles de evidencia
Algunas de las referencias bibliográficas de este resumen se acompañan del nivel de evidencia. El propósito de esto es ayudar al lector a evaluar la solidez de la evidencia que respalda el uso de ciertas intervenciones o abordajes. El
Permisos para el uso de este resumen
PDQ (Physician Data Query) es una marca registrada. Se autoriza el uso del texto de los documentos del PDQ; sin embargo, no se podrá identificar como un resumen de información sobre cáncer del PDQ del NCI, salvo que el resumen se reproduzca en su totalidad y se actualice de manera periódica. Por otra parte, se permitirá que un autor escriba una oración como "En el resumen del PDQ del NCI de información sobre la prevención del cáncer de mama se describen, de manera concisa, los siguientes riesgos: [incluir fragmento del resumen]".
Se sugiere citar la referencia bibliográfica de este resumen del PDQ de la siguiente forma:
PDQ® sobre el tratamiento para adultos. PDQ Tratamiento del melanoma ocular uveal. Bethesda, MD: National Cancer Institute. Actualización: <MM/DD/YYYY>. Disponible en:
Las imágenes en este resumen se reproducen con autorización del autor, el artista o la editorial para uso exclusivo en los resúmenes del PDQ. La utilización de las imágenes fuera del PDQ requiere la autorización del propietario, que el Instituto Nacional del Cáncer no puede otorgar. Para obtener más información sobre el uso de las ilustraciones de este resumen o de otras imágenes relacionadas con el cáncer, consultar
Cláusula sobre el descargo de responsabilidad
Según la solidez de la evidencia, las opciones de tratamiento se clasifican como "estándar" o "en evaluación clínica". Estas clasificaciones no se deben utilizar para justificar decisiones sobre reembolsos de seguros. Para obtener más información sobre la cobertura de seguros, consultar la página
Comuníquese con el Instituto Nacional del Cáncer
Para obtener más información sobre las opciones para comunicarse con el NCI, incluso la dirección de correo electrónico, el número telefónico o el chat, consultar la página del
Última revisión: 2023-08-18
Esta información no reemplaza el consejo de un médico. Ignite Healthwise, LLC, niega toda garantía y responsabilidad por el uso de esta información. El uso que usted haga de esta información implica que usted acepta los
Healthwise, Healthwise para cada decisión de la salud, y el logo de Healthwise son marcas de fábrica de Ignite Healthwise, LLC.
Page Footer
Quiero...
Audiencia
Sitios seguros para miembros
Información sobre The Cigna Group
Aviso legal
Los planes individuales y familiares de seguro médico y dental están asegurados por Cigna Health and Life Insurance Company (CHLIC), Cigna HealthCare of Arizona, Inc., Cigna HealthCare of Illinois, Inc., Cigna HealthCare of Georgia, Inc., Cigna HealthCare of North Carolina, Inc., Cigna HealthCare of South Carolina, Inc. y Cigna HealthCare of Texas, Inc. Los planes de beneficios de salud y de seguro de salud de grupo están asegurados o administrados por CHLIC, Connecticut General Life Insurance Company (CGLIC) o sus afiliadas (puedes ver
Todas las pólizas de seguros y los planes de beneficios de grupo contienen exclusiones y limitaciones. Para conocer la disponibilidad, los costos y detalles completos de la cobertura, comunícate con un agente autorizado o con un representante de ventas de Cigna. Este sitio web no está dirigido a los residentes de New Mexico.